行業(yè)動態(tài)
您當(dāng)前的位置 > 行業(yè)動態(tài) > 行業(yè)法規(guī)
PD-1市場再迎強者 價格戰(zhàn)悄然開打
加入日期:2019/6/6 11:06:00 查看人數(shù): 1348 作者:admin
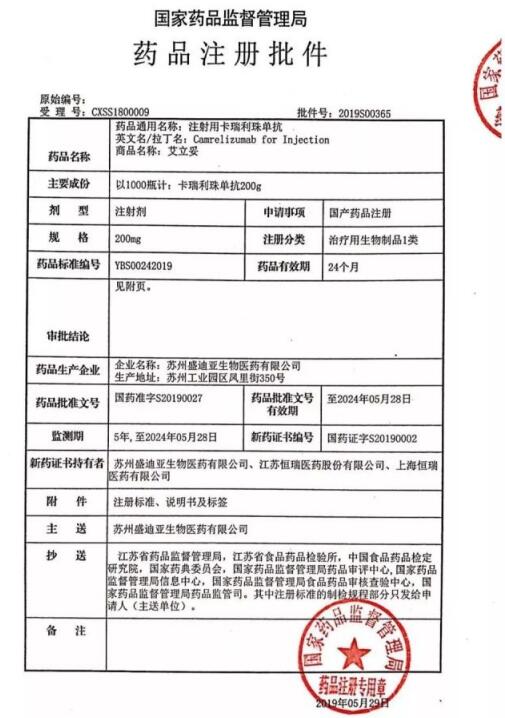
本就火熱的PD-1市場再迎強勢入局者。5月31日,恒瑞醫(yī)藥注射用卡瑞利珠單抗獲批,適用于至少經(jīng)過二線系統(tǒng)化療的復(fù)發(fā)或難治性經(jīng)典型霍奇金淋巴瘤患者的治療。至此,國內(nèi)PD-1市場已經(jīng)囊括百時美施貴寶(BMS)、默沙東、信達生物、君實生物等數(shù)家企業(yè),百濟神州等企業(yè)的相關(guān)藥品也正處于上市申請審批階段。
北京鼎臣醫(yī)藥管理咨詢中心創(chuàng)始人史立臣認為,由于獲批適應(yīng)證的不同,短期內(nèi)PD-1進入價格競爭的幾率不大,更廣泛適應(yīng)證獲批的競爭是當(dāng)前的重點,但PD-1對企業(yè)的研發(fā)實力有較高要求,“投入成本很大,實力不強的企業(yè)如果進入,結(jié)果不會太好?!?
恒瑞入局PD-1市場
恒瑞醫(yī)藥獲批的注射用卡瑞利珠單抗是人源化抗PD-1單克隆抗體,可與人PD-1受體結(jié)合并阻斷PD-1/PD-L1通路,恢復(fù)機體的抗腫瘤免疫力,從而形成癌癥免疫治療基礎(chǔ)。
通常來說,T細胞能夠殺死癌細胞,久而久之,癌細胞開始“自救”,即在表面產(chǎn)生一種特殊的蛋白質(zhì),與T細胞結(jié)合,令T細胞產(chǎn)生“錯覺”,認為癌細胞“無害”,同時使得T細胞的活性降低,這種特殊的蛋白質(zhì)就是PD-L1。癌細胞表面的PD-L1和T細胞表面的PD-1結(jié)合,會誘導(dǎo)T細胞凋亡瓦解、抑制T細胞的增殖。PD-1抑制劑和PD-L1抑制劑,通過阻斷PD-1和PD-L1的結(jié)合,使T細胞能夠正確的識別癌細胞,實現(xiàn)殺滅癌細胞的目的。因與傳統(tǒng)癌癥治療的放化療方法不同,PD-1作用于人體免疫系統(tǒng),也被認為是抗腫瘤治療的“撒手锏”。
在恒瑞入局后,國內(nèi)相關(guān)企業(yè)已經(jīng)達到5家。其中,外資企業(yè)百時美施貴寶PD-1抗體藥物歐狄沃(簡稱O藥)與默沙東PD-1抗體藥物可瑞達(簡稱K藥)均已進入內(nèi)地市場。2018年12月,首個國產(chǎn)PD-1單抗拓益獲批上市,2019年2月,信達生物PD-1信迪利單抗注射液正式上市。
前不久,“O藥”不良反應(yīng)事件給當(dāng)下正熱的PD-1市場潑了一盆冷水?!癘藥”在日本上市4年內(nèi),有11例垂體功能障礙與Opdivo存在因果關(guān)系,包括3例黑色素瘤和8例非小細胞肺癌患者,2018年11月7日,更有一例非小細胞肺癌死亡病例。百時美施貴寶隨后發(fā)布聲明稱,截至目前,在中國衛(wèi)生監(jiān)管部門所批準的適應(yīng)證范圍內(nèi),未獲悉類似潛在不良事件。與此同時,作為罕見不良反應(yīng),腦垂體炎已在全球及中國獲批適應(yīng)證產(chǎn)品說明書中標(biāo)明,用以提醒醫(yī)療專業(yè)人士發(fā)現(xiàn)并及時采取相應(yīng)措施。日本厚生勞動省要求小野藥品工業(yè)在其生產(chǎn)的抗癌藥Opdivo的使用說明中增補“重大副作用”內(nèi)容。
價格戰(zhàn)悄然開打
PD-1被認為是抗腫瘤治療的“撒手锏”,其市場規(guī)模也不容小覷。
IMS數(shù)據(jù)庫顯示,2017年P(guān)D-1抗體全球銷售額約為88.3億美元。到了2018年,這一數(shù)字已經(jīng)達141.78億美元,國內(nèi)銷售額約為643.75萬美元。6月3日,東吳證券發(fā)布研報稱,預(yù)計國內(nèi)PD-1市場空間將超過700億元。龐大的市場份額面前,各大藥企紛紛進軍PD-1市場,爭奪也從未停止。除了已經(jīng)在國內(nèi)獲批的5家企業(yè),百濟神州等企業(yè)的相關(guān)藥品正處于上市申請審批階段。
不僅如此,已經(jīng)獲批上市的企業(yè),已經(jīng)打起了價格戰(zhàn)。
2019年1月7日,首個國產(chǎn)PD-1君實生物的拓益公布了7200元/240mg(支)的定價,合30元/mg,拓益適應(yīng)證為黑色素瘤,患者年治療費用18.72萬元,再加上藥物援助方案,符合贈藥條件的患者一年治療費用預(yù)估在10萬以下。兩個月之后的3月5日,信達公布,信迪利中國地區(qū)的售價為7838元/100mg,是“K”藥(帕博利珠單抗)同等規(guī)格的四折左右,亦低于同規(guī)格的“O”藥價格。信達還同時推出“3+2”積分項目,援助后,患者每個月的治療費用約為1.39萬,年治療費用為16.7萬左右。
不僅如此,“O”藥和“K”藥在國內(nèi)的價格也幾乎是全球最低水平。K藥(黑色素瘤適應(yīng)證)價格為17918元/100mg(支),合179元/mg,患者年費用大約在60萬元。O藥價格為40mg/10ml:4591元;100mg/10ml:9260元。不同病情和體重的患者劑量和用藥不一樣,患者年均費用在30萬左右。
在北京鼎臣醫(yī)藥管理咨詢中心創(chuàng)始人史立臣看來,由于獲批適應(yīng)證的不同,短期內(nèi)PD-1價格競爭仍有限,從長遠來看,“三五年之后,隨著各PD-1在獲批適應(yīng)證上有一定的重合性,進入真正的價格競爭階段是有可能的?!?
PD-1市場的“準”競爭者并不少。2018年8月百濟神州提交了PD-1單抗的申請,獲批只是時間問題,第二梯隊方面包括正大天晴、復(fù)宏漢霖、海正藥業(yè)等十余家企業(yè),亦有涉及30余款PD-1/PD-L1單抗在研。
適應(yīng)證之爭將繼續(xù)
業(yè)界普遍認為,更廣泛適應(yīng)證的獲批,已經(jīng)成為PD-1市場的競爭重點。
在已經(jīng)獲批的產(chǎn)品方面,默沙東先人一步。2019年3月29日,“K”藥獲批了新的適應(yīng)證:聯(lián)合培美曲塞、順鉑一線治療EGFR和ALK陰性的轉(zhuǎn)移性非鱗狀非小細胞肺癌(NSCLC)。
除君實獲批適應(yīng)證為黑色素瘤外,信達、恒瑞和百濟申請的均為霍奇金淋巴瘤。
從國內(nèi)上市產(chǎn)品在國外獲批的適應(yīng)證不難看出,適應(yīng)證之爭還將繼續(xù)。以國內(nèi)最早上市的歐狄沃為例,該藥已在全球超過65個國家及地區(qū)獲得批準,在美國,歐狄沃已獲批15項適應(yīng)證,涉及非小細胞肺癌、黑色素瘤、腎癌、霍奇金淋巴瘤等8個瘤種,在日本、韓國和中國臺灣,歐狄沃胃癌適應(yīng)證也已獲得批準。
國內(nèi)企業(yè)方面,以百濟神州為例,雖然產(chǎn)品尚未正式獲批,但在適應(yīng)證領(lǐng)域的爭奪已經(jīng)展開。百濟神州高級副總裁汪來在接受新京報記者采訪時就表示,目前百濟神州已經(jīng)在進行的PD-1注冊性臨床試驗有14項,覆蓋不同的適應(yīng)證,其中有7項是全球注冊性臨床試驗?!俺艘酝猓覀兘衲赀€會展開多項PD-1的注冊性試驗,所以到今年年底,PD-1注冊性臨床試驗預(yù)計會超過14項?!蓖魜肀硎荆贊裰菰诙▋r時也會充分考慮患者的需求和可負擔(dān)性。
史立臣表示,“PD-1市場的競爭已經(jīng)成為更廣泛適應(yīng)證獲批的競爭,要增加適用人群,必然依靠適應(yīng)證范圍的擴大,但這種擴大是有速度的?!?
另一方面,對研發(fā)實力要求頗高的PD-1領(lǐng)域,對部分企業(yè)來說并不友好,單就數(shù)字而言,恒瑞醫(yī)藥在獲批產(chǎn)品項目中已投入研發(fā)費用約為5.04億元。史立臣指出,“按照目前的審批速度,到明年下半年應(yīng)該會有幾個產(chǎn)品獲批上市。投入成本很大,實力不強的企業(yè)如果貿(mào)然進入,結(jié)果不會太好。因為原研藥已經(jīng)進來了,國內(nèi)企業(yè)也在摩拳擦掌?!?
